Liposarcoma
Introducción
El término “liposarcoma” hace referencia a un conjunto de cánceres que abarca desde lesiones de comportamiento esencialmente benigno a otros de franca malignidad, más agresivos, susceptibles de recidivar y /o de metastatizar (es decir, de diseminarse). Las decisiones relativas al tratamiento y cuidados posteriores de los pacientes con liposarcomas vienen determinadas por las características y patrones de comportamiento que se conocen de los distintos subtipos existentes. Aunque muchos de los principios que rigen la evaluación y el manejo de otros tipos de sarcomas de partes blandas son sin duda aplicables al liposarcoma, éste cuenta con rasgos propios que le son únicos y que merecen una especial atención.[/vc_column_text][vc_column_text]
Historia Clínica y Examen Física
La mayoría de los pacientes con un liposarcoma acuden a consulta refiriendo la aparición de una masa, con frecuencia indolora salvo que hayan sufrido un traumatismo en la zona. Como se ha mencionado previamente, y dependiendo del lugar de origen, los lipsarcomas pueden alcanzar un tamaño bastante grande. A la palpación pueden ser blandos y carnosos o considerablemente duros; ésto depende fundamentalmente del grado de diferenciación del tumor , es decir, de en qué medida se asemeje al tejido adiposo maduro no tumoral (así, se consideran tumores bien diferenciados a aquéllos que se asemejan mucho al tejido adiposo normal). De entrada, es muy importante diferenciar los grandes lipomas benignos de los liposarcomas. Los datos que deben hacer sospechar malignidad en una masa de nueva aparición son: 1) tamaño superior a 5 cm (aproximadamente 2 pulgadas); 2) localización profunda, y 3) consistencia firme y adhesión o fijación a estructuras subyacentes (Sim 1994). Como ocurre conla evaluación de cualquier otra masa, el examen físico exhaustivo es crucial, y debe prestarse especial atención al tórax, abdomen y pelvis además de a la extremidad afectada.
Técnicas de Imagen
Tras la cuidadosa elaboración de la historia clínica y el examen físico exhaustivo se procede al estudio de la masa mediante técnicas de imagen. Para lesiones situadas en una extremidad éstas comienzan con una placa radiológica convencional (rayos X) (Sim 1994), que permitirá elucidar si existe o no afectación ósea. Seguidamente, se procede a realizar una resonancia magnética, con y sin contraste. Los liposarcomas muestran hallazgos propios y distintivos en la resonancia que permiten sugerir el diagnóstico antes incluso de la realización de una biopsia; de nuevo la especificidad de estos hallazgos depende en gran medida del grado de similitud entre la neoplasia y la grasa normal (es decir, de cuán bien diferenciada sea);
Los liposarcomas tienden a aparecer en la resonancia magnética como tumores bien delimitados, de contorno lobulado (Arkun 1997). El refuerzo tras suministro de contraste depende del grado de diferenciación. En los liposarcomas bien diferenciados el refuerzo es bajo, siendo muy superior en la variantes de células redondas, pleomórfica y desdiferenciada, todas ellas más agresivas. El liposarcoma mixoide, una variante de agresividad intermedia, muestra considerable heterogeneidad de refuerzo según las zonas en el estudio con contraste (Arkun 1997). Otros hallazgos característicos del liposarcoma son la presencia de septos fibrosos gruesos (tabiques en el interior del tumor), la nodularidad y la aparición de refuerzo con contraste en secuencias supresoras de grasa (Peterson 2003). Además, pueden observarse focos de necrosis y de hemorragia;
Antecedentes
Comparados con otros tipos de neoplasias malignas, los sarcomas de partes blandas son tumores relativamente raros. Se estima que cada año se diagnostican aproximadamente 5000 casos,lo que representa un 1% de todas las neoplasias diagnosticadas de novo en el mismo periodo (Lewis 1996).
El liposarcoma supone del 9.8 al 18% del total de sarcomas de partes blandas, siendo la segunda variante histológica en frecuencia de estos tumores; su incidencia se situa por detrás únicamente de la del fibrohistiocitoma maligno (FHM) (Peterson 2003, Enzinger 1995).
El liposarcoma es un tumor derivado de células primitivas capaces de diferenciarse hacia tejido adiposo (el que compone las grasa de debajo de la piel, y que también se encuentra alrededor de varios órganos y en torno a los músculos). Es una neoplasia propia de pacientes adultos, cuyo pico de incidencia se sitúa entre los 40 y los 60 años, y muestra una ligera prevalencia por el sexo masculino (Enzinger 1995).
Los casos aparecidos en pacientes más jóvenes tienen lugar en la segunda década de la vida (Coffin 1997, Pisters 1996). En ambos grupos de edad, la localización más frecuente es el tejido correspondiente a partes blandas profundas de las extremidades, especialmente las del muslo, donde se sitúa más del 50% del total de casos (Coffin 1997, Pisters 1996).
En esta localización debutan clínicamente como masas indoloras de crecimiento lento. Con frecuencia, estos tumores se detectan por primera vez tras traumatismos leves en el área de origen, lo que no quiere decir que el golpe los haya causado, sino que ha dirigido la atención sobre esa zona. La aparición de un bulto que no desaparece tiempo después de un traumatismo es, pues, un motivo habitual de consulta médica inicial de los pacientes con sarcomas. Desafortunadamente, dado que dichos pacientes no se sienten “enfermos” en las fases iniciales del desarrollo de su neoplasia, el diagnóstico y por consiguiente el tratamiento de los mismos se ve con cierta frecuencia demorado.
El liposarcoma fue descrito por vez primera por R. Virchow en 1857. En 1944, Arthur Purdy Scout escribió: “con seguridad, uno de los más pintorescos y fantásticos capítulos en la historia de la oncología está protagonizado por los tumores de células formadoras de tejido adiposo. Su extraña manera de crecer, su asombroso tamaño… y otros muchos rasgos peculiares…los convierten en tumores de enorme interés” (Ver R. Virchow, “Ein fall von Bosartigen zum Theil in der form des Neurons auftretenden Fettgeschwulsten,” Arch A Pathol Anat Phys, 1857, v11: pp 281-288 and “Liposarcoma—the malignant tumor of lipoblasts”, A. P. Stout, Annals of Surgery, 1944; 119( 1): pp 86-107.
Un rasgo único limitado a los liposarcomas es su tendencia a aparecer en espacios viscerales, muy especialmente en el retroperitoneo. Hasta un tercio se originan en esta localización (Peterson 2003). La presentación clínica de los liposarcomas retroperitoneales puede ser muy diferente; así, se detectan con frecuencia de forma mucho más tardía, en tanto en cuanto el espacio retroperitoneal es capaz de acomodar sin modificarse masas de tamaño muy superior a las que cabrían en el muslo. Por otra parte, en los liposarcomas retroperitoneales los síntomas de obstrucción intestinal o urinaria secundarios al crecimiento del tumor pueden dominar el cuadro clínico. El manejo de los liposarcomas de localización retroperitoneal puede ser pues particularmente dificultoso.
Es importante mencionar que, además de las localizaciones previamente descritas, el liposarcoma puede tener otros muchos orígenes. Los situados en cabeza y cuello constituyen un 5% del total mientras que los originados en la extermidad superior suponen un 10%. Otras localizaciones poco habituales incluyen el cordón espermático, la cavidad peritoneal, la axila, la vulva e incluso la mama. (Donegan 1979, Austin 1986). Si bien la gran mayoría de los liposarcomas se originan “de novo” (y no sobre otra neoplasia ya presente previamente), los de localizacion mamaria constituyen una excepción, teniendo su origen habitualmente sobre un cistosarcoma phyllodes preexistente (Donegan 1979, Austin 1986). No existe evidencia de que los liposarcomas aparezcan sobre lipomas benignos.[/vc_column_text][/vc_column][/vc_row][vc_row][vc_column width=”1/2″][vc_column_text]
Estadificación y Biopsia del Liposarcoma
Una vez que el examen físico y las pruebas de imagen llevan a un diagnóstico de sospecha de sarcoma, debe realizarse la estadificación de la enfermedad y la toma de biopsia. Ello permitirá determinar la naturaleza de la lesión y el grado de extensión (si ésta se ha producido) de la misma.
El estudio mediante técnicas de imagen de la lesión tal y como se describe previamente es parte esencial del proceso de estadificación. Además, y dado que los pulmones son el lugar más frecuente de metástasis, de forma obligada y rutinaria se realizan una radiografía convencional y un TAC de la región torácica. También se recomienda la realización adicional de un TAC de abdomen debido a la relativamente frecuente afectación del retroperitoneo y de los espacios viscerales. Deben realizarse, además, estudios de laboratorio que incluyan hemograma, velocidad de sedimentación y bioquímica elemental. Estos tests suministran conocimientos sobre la respuesta sistémica inducida por la neoplasia y al tiempo proveen de una base para la ulterior monitorización de la terapia.
La realización de una biopsia es crucial, al igual que lo es el procedimiento utilizado para la obtención de la misma, que debe permitir un diagnóstico definitivo. La histología (ésto es, la apariencia que tiene el tumor al ser examinado con el microscopio) da las primeras claves sobre su comportamiento. El tejido requerido puede obtenerse bien mediante aspiración con aguja, bien mediante biopsia abierta, de tipo incisional o excisional La biopsia abierta es una técnica quirúrgica que debe llevarse a cabo en un quirófano. Este procedimiento proporciona al patólogo la máxima cantidad de tejido para el examen; no obstante, en ocasiones no es necesario o es incluso desaconsejable. Dado que muchos de los sarcomas de partes blandas son fácilmente identificables por palpación, con frecuencia es suficiente la obtención de tejido mediante biopsia con aguja gruesa. La muestra es adquirida habitualmente por el propio radiólogo, guiado por control de imagen con tomografía computerizada (TC) o con ecografía.
En ocasiones, para obtener una nuestra de tejido adecuada es preciso llevar a cabo una biopsia incisional. Este procedimiento consiste en realizar una incisión en la piel para extraer fragmentos del tumor, que serán posteriormente evaluados. Salvo en situaciones excepcionales, la biopsia excisional (esto es, la que extirpa la totalidad del tumor como procedimiento de toma de biopsia para estudio histológico inicial) debe evitarse en casos de sospecha de sarcoma; es preferible disponer primero de una estadificación y diagnóstico histológico para planear después adecuadamente un plan terapéutico de resección completa.
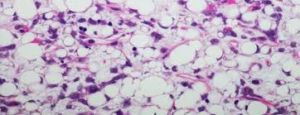
Patología del Liposarcoma
Una vez obtenido el tejido, ya se trate de una biopsia o de la pieza de extirpación completa, se realiza el examen microscópico a fin de evaluar su histología. Hay diversas técnicas especiales complementarias al estudio convencional que pueden ser de ayuda para el diagnóstico histológico preciso; su realización puede conllevar que los resultados de la biopsia tarden días y, en algunos casos, semanas en finalizarse.
La organización Mundial de la Salud (OMS) admite actualmente cuatro tipos de liposarcoma:
1) Bien diferenciado (Tumor Lipomatoso atípico)
2) Mixoide
3) Pleomórfico
4) Desdiferenciado (Christopher 2002).
Aunque estas categorías representan varios hitos de un mismo espectro de enfermedad, cada uno de ellos constituye una entidad con características propias y distintivas. En la tabla I se incluye una descripción simplificada de cada uno de los subtipos antes mencionados[/vc_column_text][vc_column_text css=”.vc_custom_1586246564130{margin-top: 50px !important;}”]
]Se ha encontrado correlación entre cierto número de alteraciones en los genes de las células malignas y los liposarcomas. Así, se ha observado que los liposarcomas bien diferenciados se asocian a anomalías de la región q13-15 del cromosoma 12 (Rubin 1997). Estas alteraciones se han encontrado también el liposarcoma desdiferenciado. La asociación genética mejor caracterizada es, probablemente, la identificada en el liposarcoma mixoide. Se trata de una traslocación o intercambio de material genético entre dos cromosomas, que en el caso del liposarcoma mixoide ocurre entre los cromosomas 12 y 16. El resultado de dicho intercambio es la creación de un nuevo gen denominado TLS-CHOP que es en realidad un oncogén, ésto es, un gen que cuando se expresa puede desencadenar el desarrollo de una neoplasia maligna. Esta traslocación específica se ha identificado únicamente en el liposarcoma mixoide siendo por tanto diagnóstica para este tumor (Rubin 1997).
Una vez caracterizado el tumor, la estadificación queda completada y puede diseñarse un plan de tratamiento adecuado. La tabla II muestra el sistema de estadificación habitualmente utilizado por los oncólogos especializados en sistema músculo-esquelético para los sarcomas de huesos y partes blandas (adaptado de Enneking 1980).[/vc_column_text][/vc_column][/vc_row][vc_row][vc_column][vc_column_text]
En la actualidad la mayoría son susceptibles de tratarse mediante cirugía conservadora del miembro. Este cambio es debido en gran parte a los avances en el conocimiento del comportamiento biológico de los sarcomas y en las técnicas de radioterapia. Los avances han conducido a una disminución en la frecuencia de amputaciones realizadas en casos de sarcomas primarios de partes blandas de un 50% a, aproximadamente, no obstante, la realización de cirugía conservadora del miembro no debe comprometer el objetivo oncológico principal, que es la curación, y debe garantizar una extremidad cuya función sea mejor que la que ofrecería una prótesis post-amputación.
Es importante señalar que, incluso tras procedimientos con conservación del miembro, pueden derivarse déficits de función. Éstos pueden variar significativamente dependiendo del tamaño y la localización del tumor, y son debidos a la extirpación de tejidos situados en la inmediata vecindad del tumor (músculos, nervios, tendones, etc). En algunos casos, es posible realizar una reconstrucción de los déficits post-resección
Radioterapia y Quimioterapia Para el Liposarcoma
Aunque con terapia combinada, que incluye cirugía y radioterapia, se han alcanzado tasas de control local del 85-90% (Spiro 1997), el momento de aplicación de la radioterapia, antes o después de la cirugía, continúa siendo un aspecto discutido. La radiación preoperatoria tiene la ventaja de permitir el suministro de menores dosis en un campo más reducido. Además, el tumor puede disminuir realmente de tamaño tras su aplicación, haciendo más factible técnicamente la cirugía. En contrapartida, las complicaciones quirúrgicas se incrementan , especialmente las relacionadas con el área de incisión. Pollak et al (1998) han publicado complicaciones en la cicatrización de la herida quirúrgica del 25%, frente al 6% observado en los pacientes que recibieron tratamiento radioterápico post-operatorio. Se ha sugerido, no obstante, que la mejora en el pronóstico oncológico de los pacientes con liposarcomas y la disminución de la incidencia de complicaciones tardías permanentes justificaría el uso de la radioterapia preoperatoria, a pesar de la mayor tasa de complicaciones (Virkus 2002). El papel de la quimioterapia en el tratamiento del liposarcoma continúa siendo controvertido; de forma óptima, su utilización debe valorarse en cada caso individual.
En relación al liposarcoma, lo comúnmente aceptado es que el comportamiento de un tumor en concreto depende del subtipo histológico de éste (ver más arriba). Los liposarcomas bien diferenciados tratados con cirugía y radioterapia perioperatoria (antes o después de la cirugía) tienen una tasa de recidiva local inferior al 10% y un índice de metástasis muy cercano al 0% (Zagars 1996). Por el contrario, los liposarcomas pleomórficos recaen en un tercio de los casos y se diseminan en un 40%. Las tasas de supervivencia a los 5 y 10 años para los pacientes con liposarcomas son del 100% y 87% para la variante bien diferenciada, del 88% y 76% para el tipo mixoide y del 56% y 39% para la variante pleomórfica (Zagars 1996, Chang 1989).
La recaída local depende en gran medida del estado de los márgenes en la pieza quirúrgica; los márgenes afectados por el tumor se asocian a una alta tasa de recidiva (Sadoski 1993) y, por tanto, a un pronóstico desfavorable (Spiro 1997). En algunas situaciones, la amputación es aún el tratamiento de elección para los pacientes con sarcoma, aunque no es completamente efectiva como protección frente la recidiva local En caso de requerirse la amputación, el paciente optará con frecuencia por el uso de una prótesis, cuya selección dependerá del nivel al que la amputación ha sido realizada. De forma resumida, cuantas más articulaciones sanas pueda conservar el paciente, mejor será su función motriz. Los elementos esenciales para llevar con éxito la transición al uso de un miembro protésico incluyen la participación de un profesional protésico competente, la realización diligente de un programa de rehabilitación que incluya los cuidados postquirúrgicos del muñón y el entrenamiento en deambulación y, lo más importante, una verdadera implicación del paciente en el proceso.
Seguimiento
Una vez extirpado el tumor y completada la terapia adyuvante (la radioterapia y, más rara vez, la quimioterapia), es necesario un seguimiento continuado a fin de detectar con prontitud cualquier evidencia de recaída local o de metástasis . Ésto incluye la exporación cuidadosa, los rayos X de la extremidad afectada y estudios seriados por imagen (habitualmente mediante tomografía computerizada, TAC) de tórax y abdomen, incluyendo la pelvis si existe indicación para ello. Este seguimiento continúa, si bien con ciertas modificaciones, durante el resto de la vida del paciente. En caso de detectar recidiva o metástasis, se aplicará el tratamiento oportuno.
Una complicación que acontece en ocasiones es la aparición de un sarcoma inducido por radiación. Por definición, se trata de tumores que se originan en tejidos irradiados previamente que se encontraban libres de tumor antes de la radiación. Estas neoplasias aparecen al menos 2 o 3 años después de finalizado el tratamiento, pudiendo aparecer hasta 30 años más tarde. La variante histológica más frecuente es el Sarcoma Pleomórfico Indiferenciado, un tumor típicamente de alto grado, que supone un 70% del total de casos. La tasa de supervivencia de estas neoplasias se sitúa en un 5-26% (Robinson 1988, Laskin 1988).
Conclusión
El término “liposarcoma” hace referencia a un conjunto de neoplasias cuyo comportamiento depende del subtipo histológico. Las directrices principales del tratamiento son, sin embargo, esencialmente idénticas a las de otros sarcomas de partes blandas. En términos generales éstas incluyen una combinación de cirugía y radioterapia, con o sin quimioterapia. Es fundamental en estas neoplasias realizar un riguroso examen del paciente a fin de descartar cualquier signo de recaída local o de metástasis; y cualquier nueva dolencia notada por el paciente debe de ser así mismo referida con prontitud. Esto es especialmente importante en el caso del liposarcoma, que puede cursar con patrones de diseminación y recidiva inusuales (Vassilopoulos 2001, Linehan 2000, Pearlstone 1999).
[/vc_column_text][/vc_column][/vc_row][vc_row][vc_column width=”1/2″][/vc_column][vc_column width=”1/2″][/vc_column][/vc_row]

